[2017 노벨 생리의학상] 생체시계의 원리를 밝히다
지난 2일, 노벨 위원회가 발표한 2017년 노벨 생리의학상의 영광은 생체시계의 원리를 밝힌 제프리 홀, 마이클 로스바쉬, 마이클 영에게 돌아갔다. 노벨 위원회는 생체시계를 조절하는 작동 메커니즘을 밝힌 공로로 수상자들을 선정했다고 밝혔다.
생체시계란 낮과 밤의 24시간 주기에 따른 동식물의 다양한 생리, 대사 등의 리듬을 담당하는 일종의 생물학적 시계이다. 해외여행 시 시차적응이 어려운 것은 이 생체시계와 외부환경의 부조화로 인한 것이며, 생체시계와 반대되는 일상생활을 지속하는 것은 알츠하이머, ADHD, 우울증 등의 질병에 걸릴 위험을 높일 수 있다. 이렇듯 건강과도 밀접한 관련을 지니고 있어 생체시계는 중요한 연구 대상이기도 하다.
생체시계의 존재는 이미 오래 전부터 알려져 있었다. 18세기에 장 자크는 낮에는 잎을 펴고 밤에는 잎을 닫는 미모사를 암실에 넣어도 그대로 낮과 밤이 있는 것처럼 미모사의 생체리듬이 유지되는 것을 관찰했다. 이 연구를 통해 식물들에게 외부 환경과는 독립적으로 작용하는 내부의 생체시계가 있다는 것은 밝혀졌지만, 그것이 어떻게 작동하는지는 미지수였다. 1970년대에 시모어 벤저는 초파리에서 생체시계를 조절하는 유전자가 있을 것이라 생각했다. 그는 특정 유전자에 변이가 일어나면 초파리의 생체시계에 이상이 생기는 것을 보이고, 이 유전자를 ‘period’라고 명명하였다. 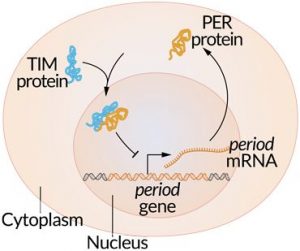
올해의 노벨 생리의학상 수상자들은 초파리에서 이 period 유전자를 분리하고, 또 이 유전자의 정보를 담고 있는 단백질인 PER이 밤에 축적되고, 낮에 감소하는 것을 알아내었다. 그렇다면 이 생체 주기는 어떻게 유지되는 것일까? 제프리 홀과 마이클 로스바쉬는 음성 피드백 기전을 그 가설로 세웠다. 즉, PER 단백질의 양이 증가하면 이것이 period 유전자의 활성을 저하시킨다고 생각한 것이다. 그러나 이 가설은 PER 단백질이 어떻게 핵 속으로 들어가 유전자의 활성을 막는지는 설명하지 못했다. 이들은 밤에 핵 속에 PER 단백질이 축적되는 것은 확인하였으나, 세포질에서 생성된 단백질이 다시 핵 속으로 들어가는 메커니즘은 밝히지 못한 것이다. 1995년, 마이클 영이 TIM 단백질을 만드는 두 번째 생체시계 유전자인 ‘timeless’를 발견하면서 이 문제는 해결되었다. TIM이 PER에 가서 붙으면, 두 단백질은 세포의 핵에 들어가 period 유전자의 활성을 막을 수 있었다.
음성 피드백의 원리를 밝혔음에도 남아 있던 또 다른 의문은 이 피드백의 주기는 어떻게 결정되느냐였다. 마이클 영은 ‘doubletime’이라는 또 다른 유전자의 존재를 밝혀내었고 이 유전자의 정보를 담고 있는 DBT 단백질이 PER 단백질의 축적을 지연시킴으로써 주기 조절에 관여한다는 것을 알아내었다.
이번 수상자들의 가장 큰 공로는 이와 같이 생체시계의 핵심적인 메커니즘을 밝힌 데 있으며, 그 밖에도 이들은 period 유전자의 활성에 필요한 단백질들의 존재를 알아내고 빛이 생체시계를 활성화하는 메커니즘 또한 규명한 바 있다. 수상자들은 해당 연구를 통해 생체시계에 관한 완전한 이해를 도움으로써 생체리듬치료와 같은 새로운 치료 전략의 길을 열고, 시간생물학(chronobiology)의 새로운 패러다임을 연 것으로 평가되고 있다.
알아두면 쓸모 있는 노벨 생리의학상 후보들
CRISPR(유전자 가위) : 크리스퍼는 주기적 간격을 띠고 분포하는 짧은 회문 구조의 반복서열로, 유전자 가위의 역할을 하여 생물의 유전체를 수정할 수 있게 해 준다. 아직은 고등 생물의 유전체를 수정할 수는 없으나, 멸종 생물 복원이나 새로운 치료법 개발 등 그 활용 가능성은 무궁무진하다.
면역 항암 요법 : 면역 항암 요법은 인체의 면역 체계를 활성화하여 암세포와 싸우게 하는 새로운 암 치료의 패러다임으로, 암세포가 T세포의 공격을 회피하기 위해 보내는 면역회피신호를 차단하여 T세포가 암세포를 원활하게 파괴할 수 있도록 하는 방법이다.
*생체시계 관련 내용은 노벨 위원회의 언론 발표 자료를 참고로 번역, 요약한 것임을 밝힙니다.
남현서 기자/연세원주
<che1027@naver.com>